


发布时间: 2024-05-31
2024年3月12日,神经与肿瘤药物研发全国重点实验室自主研发的人源化GPRC5D-BCMA-CD3三特异性抗体SIM0500的新药临床试验申请(IND)于本周内接连获得美国食品药品管理局(FDA),以及中国药品监督管理局(NMPA)批准,将开展用于复发或难治性多发性骨髓瘤患者的临床研究。
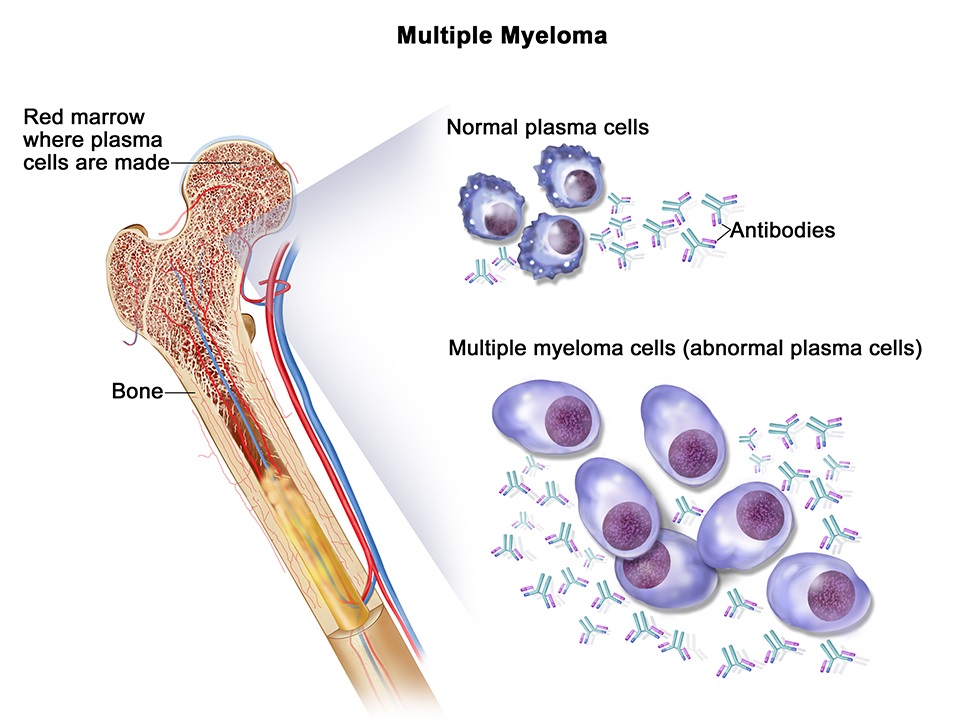
多发性骨髓瘤(multiple myeloma,MM)是血液系统第二大恶性肿瘤,主要特征是浆细胞 (即骨髓瘤细胞) 的恶性克隆并浸润骨骼及软组织,产生异常免疫球蛋白 (M蛋白) 及其多肽链。临床主要表现为骨骼疼痛,病理性骨折,肾功能损害,贫血和高钙血症。目前有多种不同作用机制药物获批并广泛用于临床,包括烷化剂、类固醇、蛋白酶体抑制剂、免疫调节药物、组蛋白去乙酰化酶抑制剂、单克隆抗体和选择性核输出抑制剂等的联合治疗,也可与高剂量化疗和自体干细胞移植联合使用。尽管MM的预后随着新疗法获批,获得了很大的改善,但该疾病目前仍然难以治愈,患者仍需更有效、可负担的治疗选择。
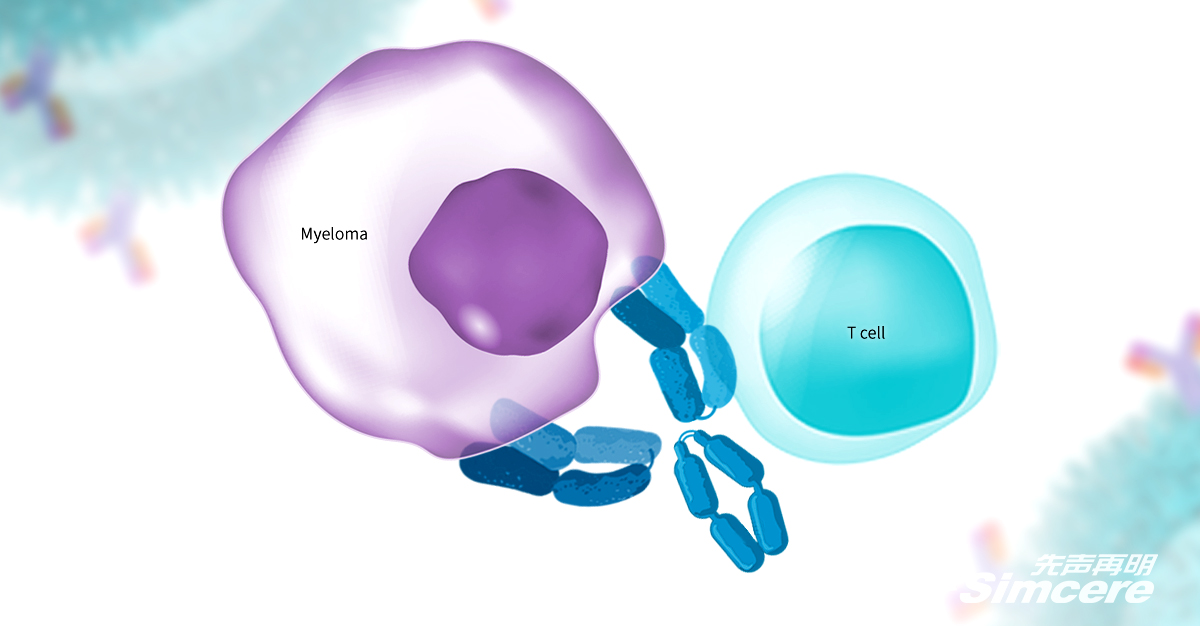
SIM0500是一种人源化GPRC5D-BCMA-CD3三特异性抗体,在中美两国同步开发。该分子通过实验室自有的T细胞衔接器多特异性抗体技术,以低亲和力高靶向激活的CD3抗体,与抗肿瘤相关抗体(GPRC5D、BCMA)组合,形成特异性靶向肿瘤的T细胞激活药物,具有多个抗体效应的协同作用。在临床前研究中,SIM0500显示出肿瘤杀伤效果显著,耐受性好,起效剂量低,停药后肿瘤不复发等多重优势,有望克服现有治疗手段所导致的耐药,具有成为多发性骨髓瘤治疗同类最佳候选药物的潜质。